武汉贝茵莱生物科技有限公司
入驻年限:10 年
- 联系人:
黄经理
- 所在地区:
湖北 武汉市
- 业务范围:
试剂、医疗器械、技术服务、耗材、实验室仪器 / 设备、书籍 / 软件、原辅料包材、细胞库 / 细胞培养
- 经营模式:
生产厂商 经销商 科研机构 代理商
推荐产品
新闻中心/正文
一区TOP:中山大学第三附属医院发现一种Cu NZs@PLGA纳米纤维和dECM水凝胶的协同疗法可有效治疗急性肝衰竭
人阅读 发布时间:2023-09-12 10:50

2023年5月,中山大学第三附属医院纳米医学中心生物材料与转化医学实验室李明强课题组,开发了一种协同治疗平台,由Cu- NZs负载的PLGA纳米纤维(Cu NZs@PLGA纳米纤维)和dECM水凝胶组成,用于递送人脂肪来源的间充质干细胞/基质细胞来源的HLCs (HADMSCs来源的HLCs),经研究证实可有效治疗ALF。
课题组在高水平期刊《Bioactive Materials》(IF:18.9,中科院1区)发表了题为“Stem cell-derived hepatocyte therapy using versatile biomimetic nanozyme incorporated nanofiber-reinforced decellularized extracellular matrix hydrogels for the treatment of acute liver failure (使用多功能仿生纳米酶结合纳米纤维的干细胞来源的肝细胞疗法可促进脱细胞细胞外基质水凝胶治疗急性肝衰竭)”的原创性研究论文。

Bioswamp®贝茵莱生物为客户提供anti-ATP-binding cassette sub-family C member 2 (ABCC2) antibody、anti-dipeptidyl peptidase 4 (DPP4) antibody等抗体产品,列表如下:
| 靶标/产品名称 |
货号 |
| MRP2/ABCC2 Polyclonal Antibody |
PAB35870 |
| CD26/DPP4 Polyclonal Antibody |
PAB32046 |
研究背景
急性肝衰竭(ALF)是一种广泛存在的危及生命的疾病肝细胞坏死和肝功能急性恶化,除了肝移植,目前仍然没有治疗ALF的满意方法。随着生物技术和纳米科学的快速发展,各种具有酶模拟活性的纳米材料,即纳米酶,引起了人们极大的兴趣。氧化铜纳米酶(Cu NZs)是一类具有保护细胞免受氧化应激损伤的纳米材料,但传统的静脉给药不仅影响治疗效果还可能引起潜在的副作用,而PLGA静电纺丝纳米纤维容易被纳米酶功能化,并且不影响纳米酶清除ROS的活性,由此认为使用PLGA静电纺纳米纤维原位递送Cu NZs可能是有效清除ALF肝脏中过量ROS的替代解决方案。
间充质干细胞(Mesenchymal stem/stromal cells, MSCs)具有多系分化潜力、自我更新能力以及抗氧化和抗炎功能,临床转化中也表现出低免疫反应,没有伦理问题。间充质干细胞衍生的肝细胞样细胞(HLCs)作为肝细胞治疗的替代细胞来源显示出巨大的潜力,但在静脉注射后易被肺部阻塞,或在脾内移植后被巨噬细胞/吞噬细胞清除,细胞植入的炎症环境也可导致移植细胞坏死和凋亡。肝脱细胞细胞外基质(dECM)水凝胶可为被包裹的细胞提供了类似naïve肝脏的微环境且没有不良免疫反应,引起了人们的高度关注,但dECM水凝胶的机械强度较弱,且损伤部位的微环境恶劣,这对移植的HLCs的正常功能构成了挑战。
研究结果
#1.
如图1所示,Cu NZs可成功嵌入到PLGA纳米纤维中,Cu NZs@PLGA纳米纤维表现出较高的拉伸强度,并能够有效去除H2O2、-OH和O2-。
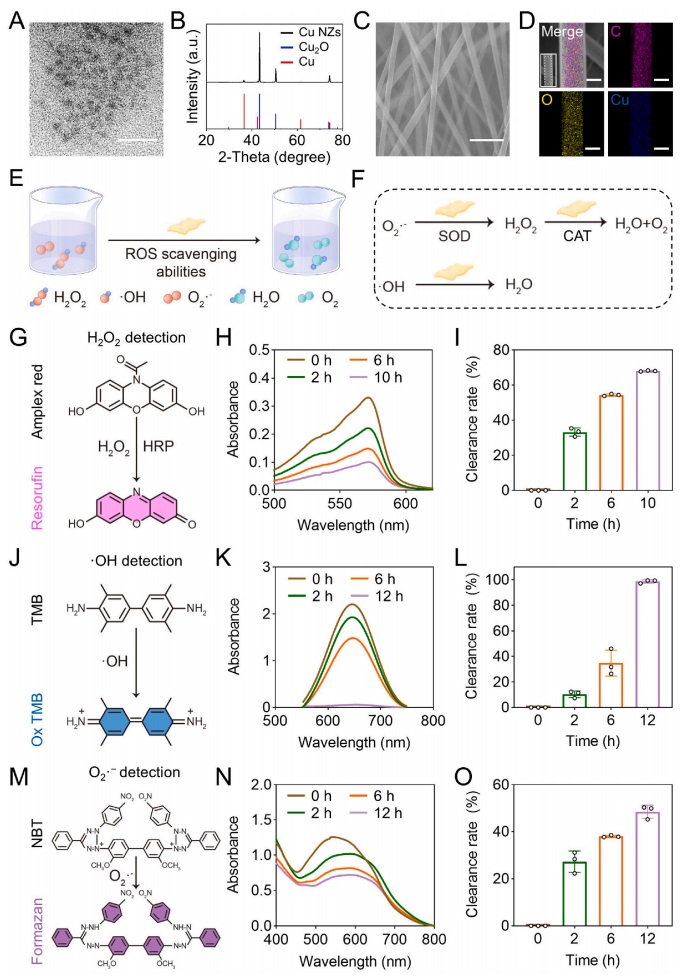
图1 Cu NZs和Cu NZs@PLGA纳米纤维的表征
#2.
如图2所示,体外研究发现,Cu NZs@PLGA纳米纤维不仅能明显促进高ROS条件下肝细胞的存活,减轻氧化应激引起的细胞损伤,还能促进HUVECs细胞的迁移和增殖,表现出促血管生成作用。
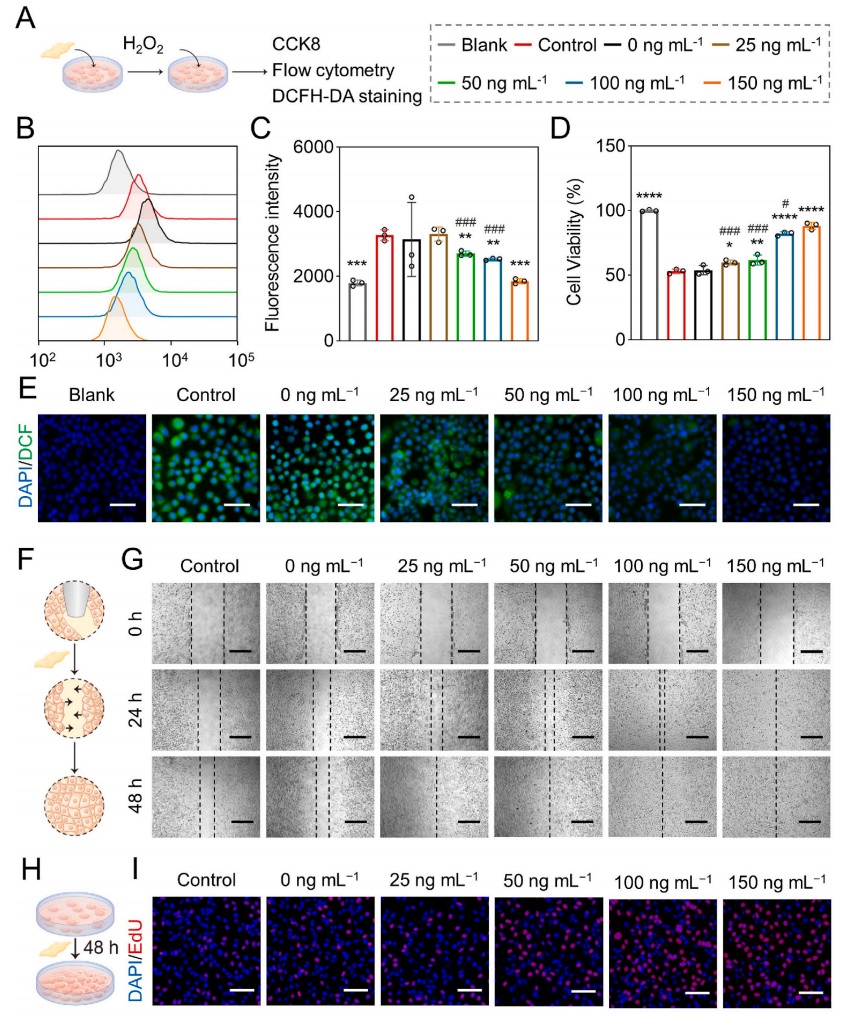
图2 Cu NZs@PLGA纳米纤维体外清除活性氧活性研究
#3.
多能间充质干细胞可以通过不同的方法诱导向肝脏谱系发展,如图3所示,研究发现hADMSCs可被成功诱导为具有典型肝细胞相关形态和功能的HLCs,有利于改善ALF的肝脏生物功能。
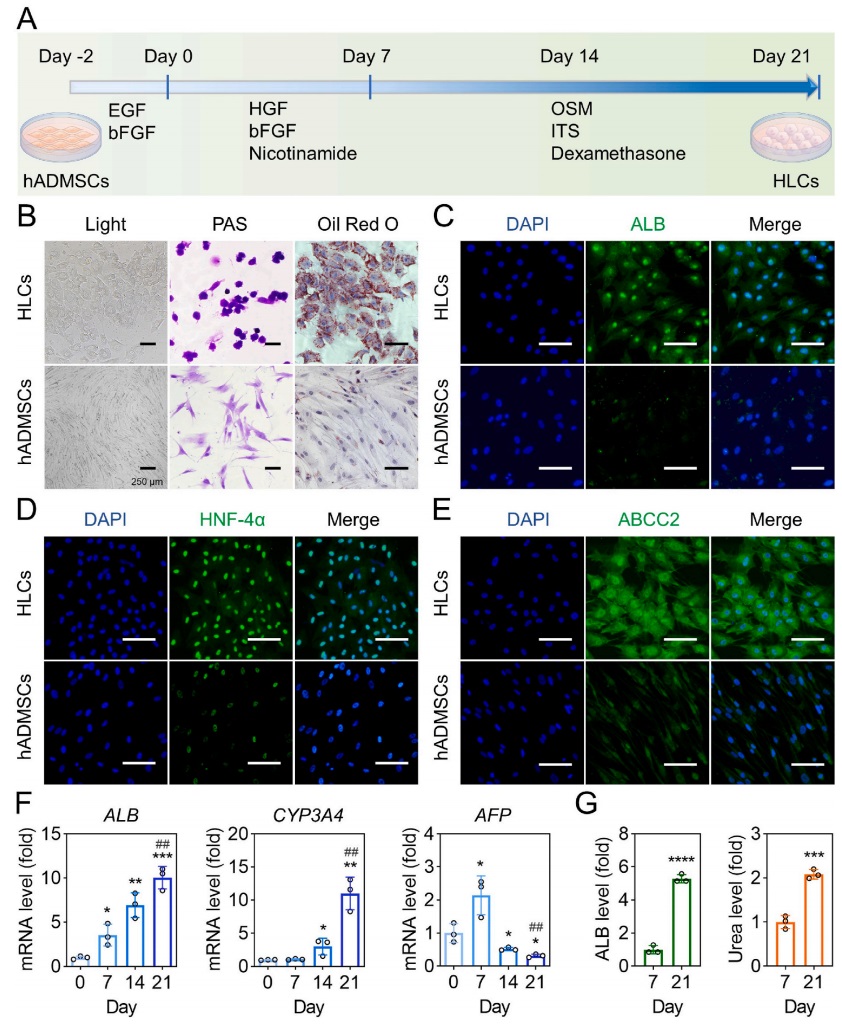
图3 hADMSCs衍生的HLCs的表征
#4.
如图4所示,本研究评价了HLCs上清对巨噬细胞极化的影响,研究发现HLCs上清液可逆转炎症状态下巨噬细胞的极化,使巨噬细胞发生M2极化(抗炎表型),由此认为在ALF治疗中,诱导的HLCs可能通过提高宿主肝细胞的抗氧化和细胞活力来促进肝脏再生。
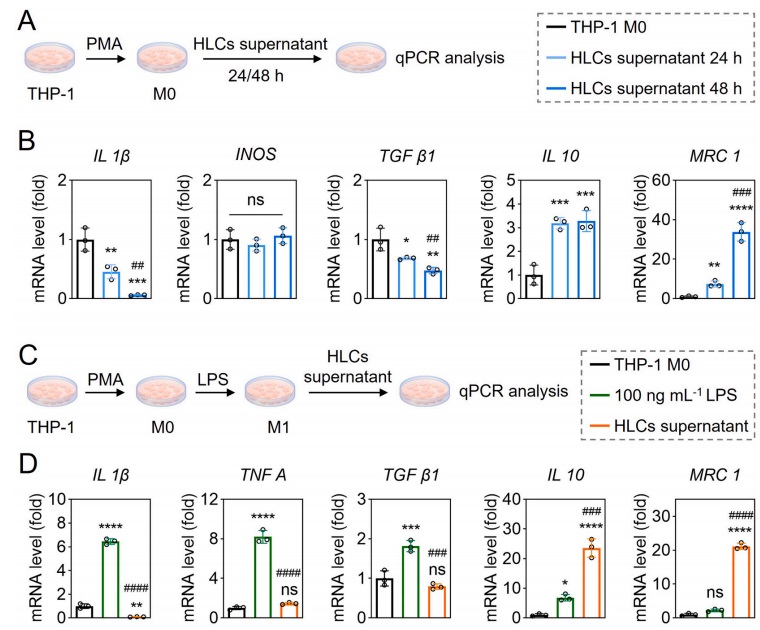
图4 HLCs上清对巨噬细胞极化的影响
#5.
为了高效地原位递送HLCs,本研究中使用了肝dECM水凝胶,如图5所示,研究发现,dECM水凝胶有利于维持HCC表型和增强肝细胞相关功能,Cu NZs@PLGA纳米纤维不仅可作为dECM水凝胶的机械支撑,还能对dECM水凝胶中嵌入的HLCs的细胞发挥保护作用。
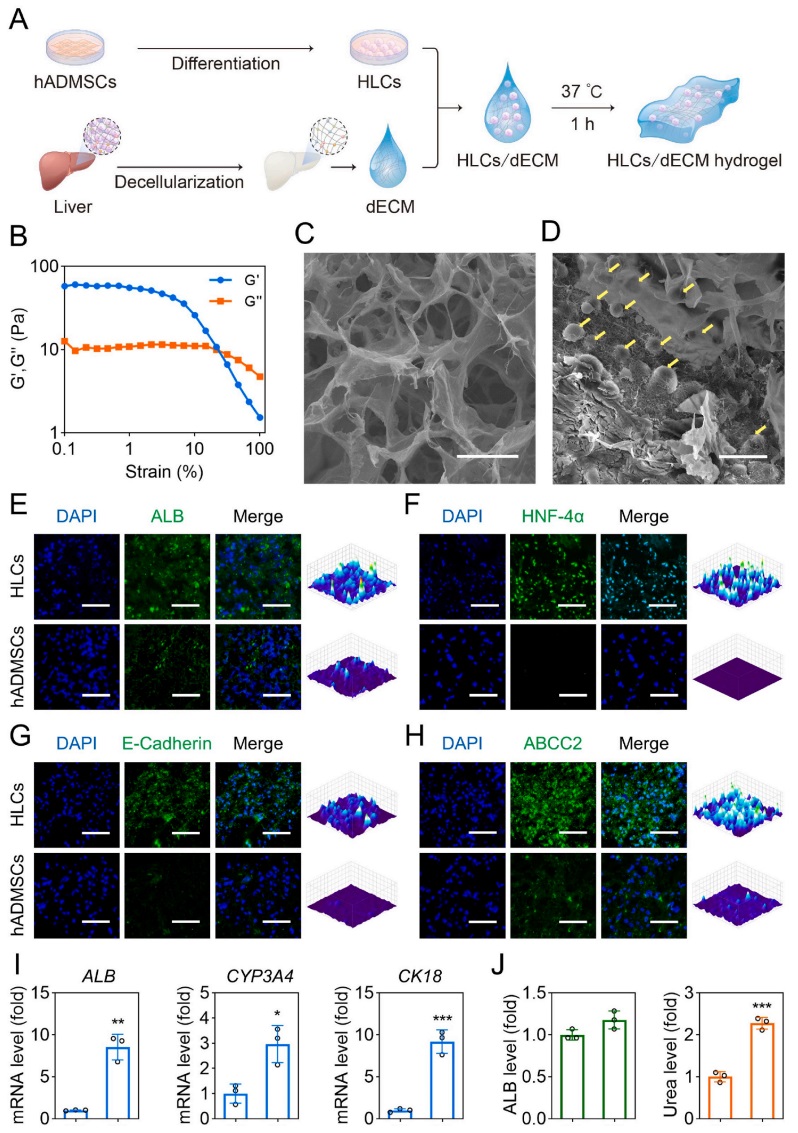
图5 Cu NZs@PLGA纳米纤维
增强dECM水凝胶的表征和功能
#6.
在体内,基于CCL4诱导的ALF模型,评价了HLCs/Cu NZs@fiber/dECM的协同治疗效果,如图6所示,研究发现Cu NZs@PLGA纳米纤维可增强dECM水凝胶递送HLCs用于ALF治疗,与hADMSCs/Cu NZs@fiber/dECM相比,CCl4诱导的ALF小鼠模型相比,移植了HLCs/Cu NZs@fiber/dECM的小鼠出现了更少的组织坏死和更明显的细胞增殖,这表明移植的HLCs具有替代肝脏功能和对宿主肝细胞的优质保护作用的重要性。
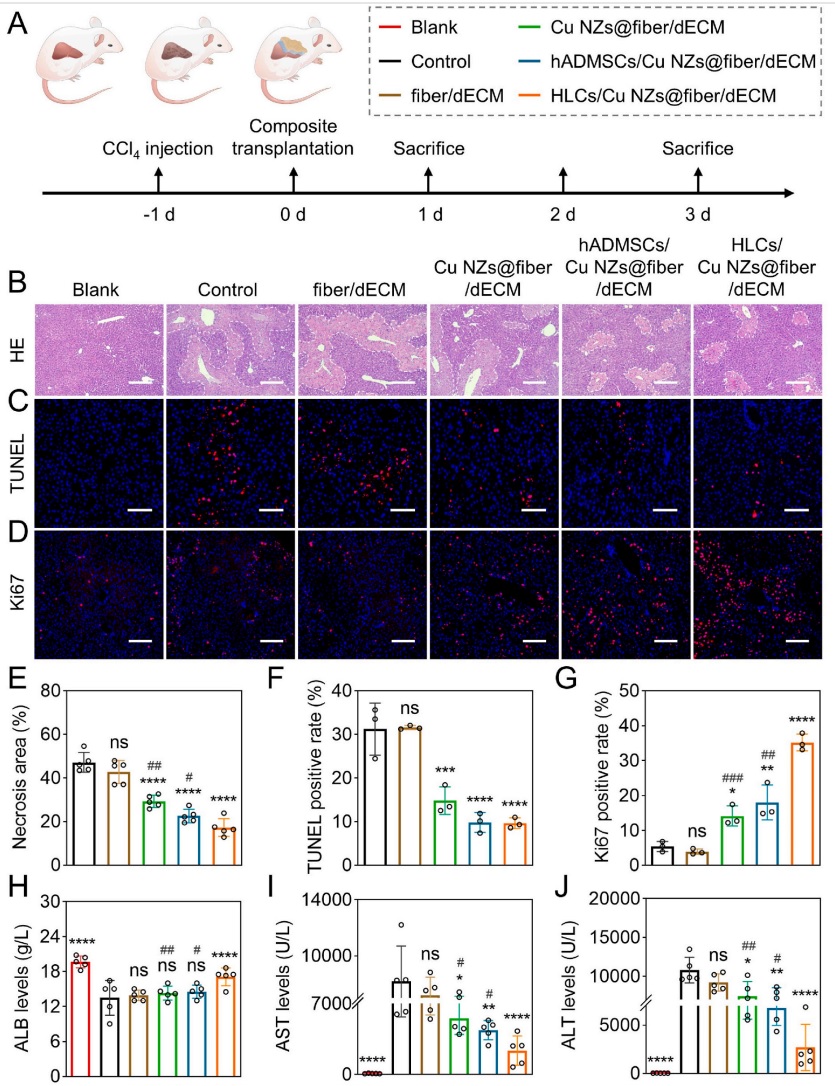
图6 HLCs/Cu NZs@fiber/dECM治疗
对ALF小鼠肝脏的保护作用
#7.
如图7所示,进一步研究发现,HLCs/Cu NZs@fiber/dECM在体内具有据好的抗炎作用,并表现出促血管生成作用。
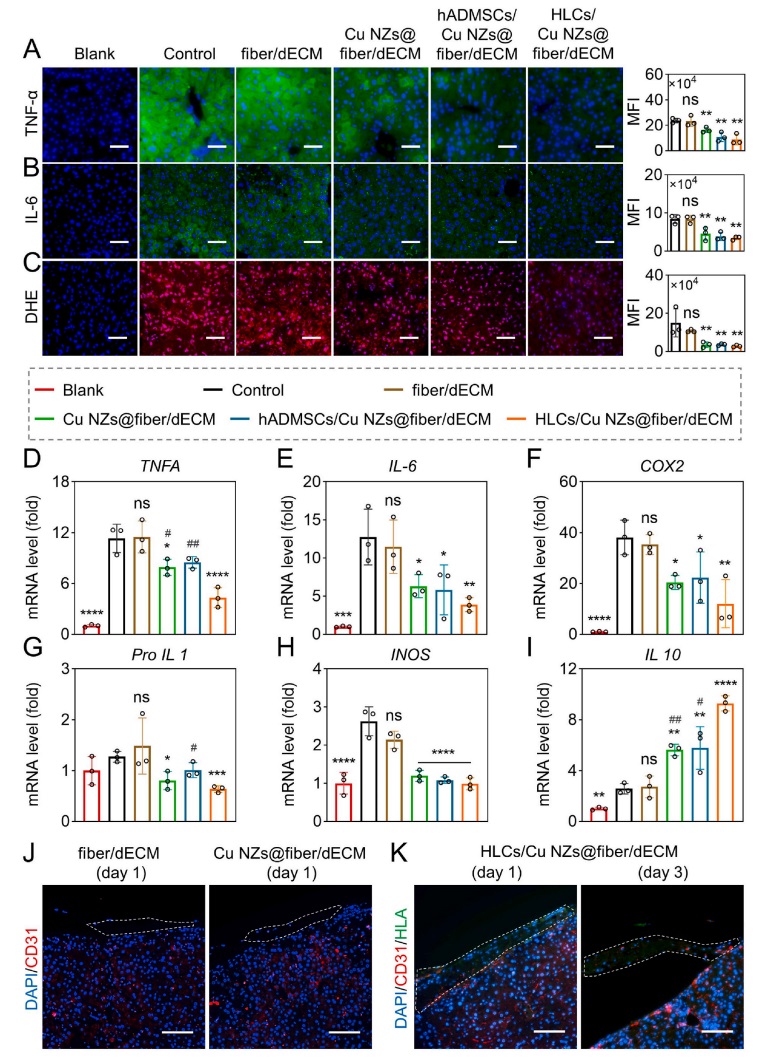
图7 HLCs/Cu NZs@fiber/dECM治疗对ALF小鼠肝脏
炎症水平及血管生成的影响
#8.
为了进一步研究HLCs/Cu NZs@fiber/dECM的治疗机制,收集肝组织进行转录组分析,如图8所示,研究发现在植入HLCs /Cu NZs@fiber/dECM的小鼠肝脏中,炎症或氧化应激相关基因显著下调,抗氧化基因、血管生成相关基因及肝再生相关基因的表达均明显升高。
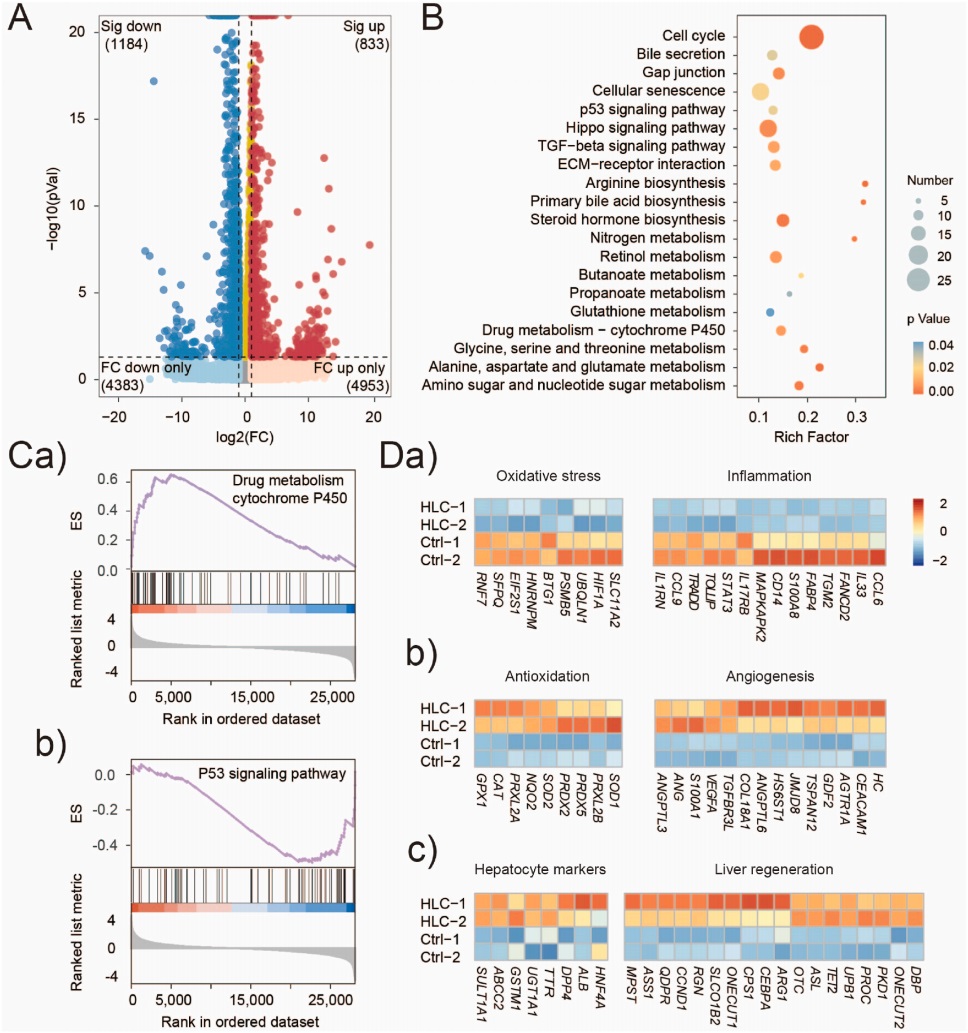
图8 转录组分析揭示
HLCs/Cu NZs@fiber/dECM的治疗机制
研究结论
该团队开发的一种Cu NZs@PLGA纳米纤维增强的dECM水凝胶,可用于原位递送功能性HLCs,具有较高的活性氧清除效率,可减少组织坏死和炎症,促进肝脏再生和功能恢复,是治疗ALF的一种很有前景的方法,并且具有巨大的临床转化潜力。
—THE END—






